As moléculas são como pequenos blocos de construção formados por átomos unidos. Elas podem ser simples, como o oxigênio que respiramos, ou muito complexas.
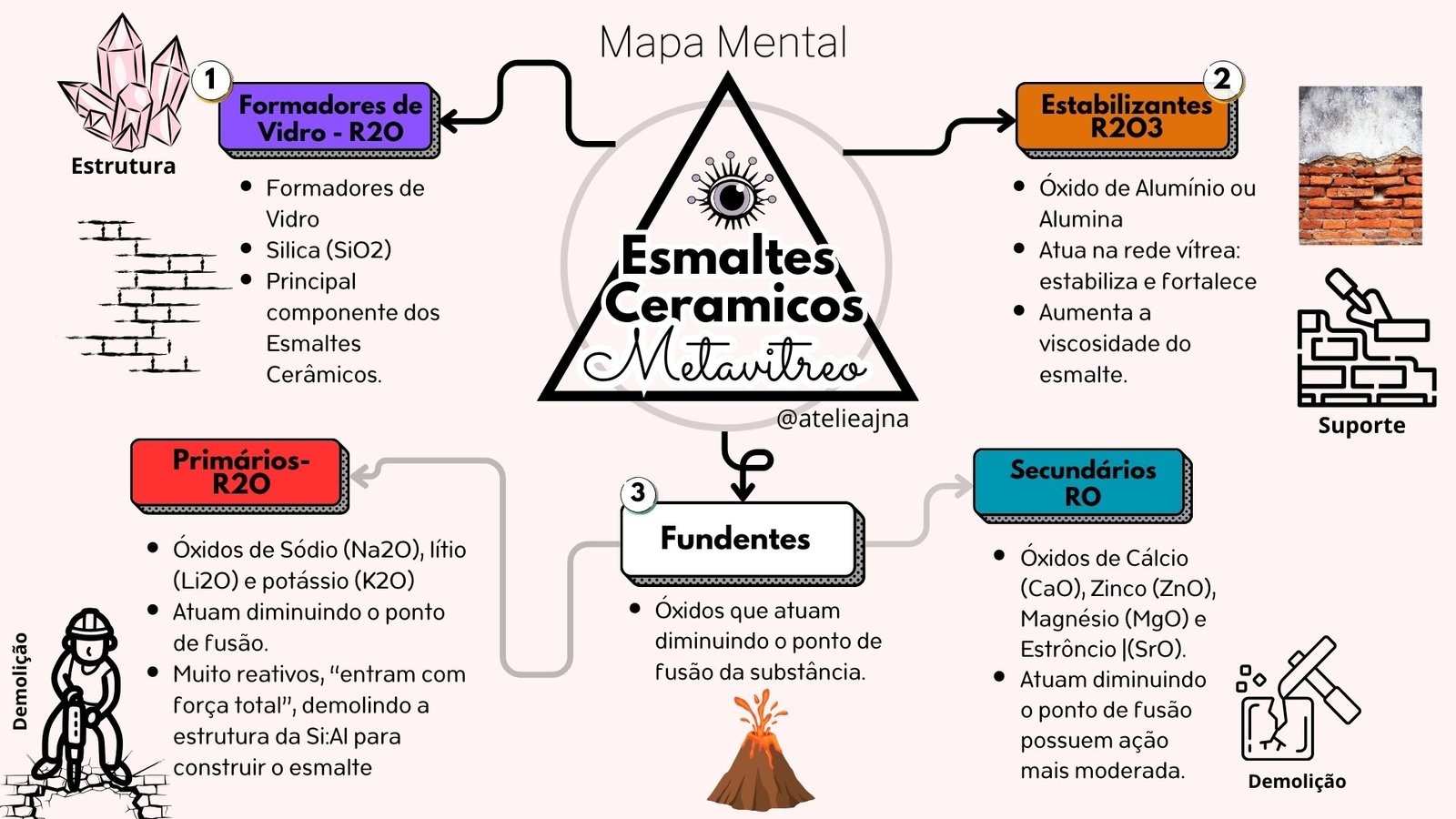
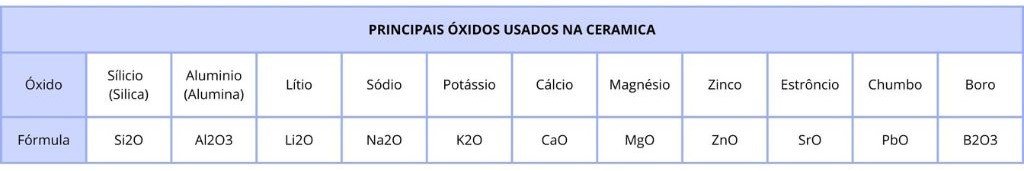
Ao criar esmaltes para cerâmicas, a mágica acontece no mundo minúsculo das moléculas. Imagine-as como ingredientes que se misturam para formar novas substâncias. Uma combinação muito comum em cerâmicas é a de metais com oxigênio, formando os chamados óxidos.
Nas cerâmicas, esses óxidos geralmente se unem por uma força de atração muito forte entre cargas opostas, formando uma estrutura bem organizada. Essa força especial é chamada de ligação iônica. É como se os metais “doassem” elétrons e o oxigênio os “recebesse”, criando uma espécie de imã microscópico entre eles.
No entanto, nem sempre as ligações nas cerâmicas são assim. Em alguns casos, os átomos podem compartilhar elétrons (ligação covalente) ou até mesmo formar uma “nuvem de elétrons” compartilhada por todos os átomos (ligação metálica).
Essa variedade de ligações explica por que as cerâmicas apresentam propriedades tão diferentes. Por exemplo, a força das ligações influencia a dureza e a resistência ao calor da cerâmica. Já a forma como os elétrons se comportam pode determinar se a cerâmica conduz eletricidade ou não.
Em resumo, as moléculas e as diferentes formas como elas se unem são fundamentais para entender as propriedades das cerâmicas e de muitos outros materiais ao nosso redor.